Membres de l'équipe
Elena Brunet
Douleur chronique : mécanismes moléculaires et cellulaires.
Notre équipe explore les mécanismes par lesquels les lésions tissulaires et nerveuses produisent des changements dans le système nerveux périphérique et central, entraînant une douleur persistante..
La douleur chronique affecte un tiers de la population mondiale créant une énorme souffrance et un handicap. Son coût sociétal est supérieur à celui du diabète, du cancer et des maladies cardiaques réunis. Malgré ces faits, on sait très peu de choses sur la façon dont la douleur devient chronique. Des preuves croissantes suggèrent que la la perte de l’inhibition spinale (désinhibition). est l’un des plus importants mécanismes sous-jacents de la douleur chronique. L’objectif de notre équipe est de déchiffrer les mécanismes moléculaires et cellulaires qui sous-tendent la transition de l’aigu au chronique. Pour répondre à ces questions, nous utilisons une approche multidisciplinaire combinant la génétique de la souris, la pharmacologie comportementale, les omiques et l’électrophysiologie ex-vivo.. En particulier, (i) nous étudions le rôle de TAFA4 ; une neurokine sécrétée enrichie en C-LTRMs dans la modulation de l’activité des neurones gating,. (ii) nous abordons le rôle des C-LTMRs eux-mêmes dans la modulation de la douleur mécanique induite par une blessure,. (iii) nous étudions comment la perte de fonction d’une protéine myosine atypique enrichie de l’intestin (Myo1a) prédispose les souris à développer des douleurs chroniques de manière sexuellement dimorphique.. Notre équipe s’intéresse également de plus en plus à la compréhension des mécanismes moléculaires et cellulaires qui sous-tendent les différences liées au sexe dans la douleur chronique.
Publications
TAFA4 relieves injury-induced mechanical hypersensitivity through LDL receptors and modulation of spinal A-type K + current
Sensory neuron-derived TAFA4 promotes macrophage tissue repair functions
Loss of bhlha9 impairs thermotaxis and formalin-evoked pain in a sexually dimorphic manner
GINIP, a Gαi-Interacting Protein, Functions as a Key Modulator of Peripheral GABAB Receptor-Mediated Analgesia.
TAFA4, a Chemokine-like Protein, Modulates Injury-Induced Mechanical and Chemical Pain Hypersensitivity in Mice
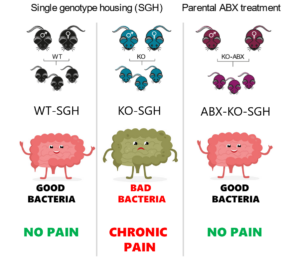
Gut microbiota promotes pain chronicity in Myosin1A deficient male mice
A novel Nav1.8-FLPo driver mouse for intersectional genetics to uncover the functional significance of primary sensory neuron diversity
Sex-related exacerbation of injury-induced mechanical hypersensitivity in GAD67 haplodeficient mice.
Diverse roles and modulations of I A in spinal cord pain circuits
TAFA4 relieves injury-induced mechanical hypersensitivity through LDL receptors and modulation of spinal A-type K + current
TrkA specific signalling pathways are critical for mechanical allodynia development and bone alterations in a mouse model of rheumatoid arthritis
Sensory neuron-derived TAFA4 promotes macrophage tissue repair functions
Loss of bhlha9 impairs thermotaxis and formalin-evoked pain in a sexually dimorphic manner
A cell fitness selection model for neuronal survival during development
5-oxoETE triggers nociception in constipation-predominant irritable bowel syndrome through MAS-related G protein-coupled receptor D
TAFA4 Reverses Mechanical Allodynia through Activation of GABAergic Transmission and Microglial Process Retraction
Disruption of TRPV3 Impairs Heat-Evoked Vasodilation and Thermoregulation: A Critical Role of CGRP
Genetic ablation of GINIP-expressing primary sensory neurons strongly impairs Formalin-evoked pain.
The Low-Threshold Calcium Channel Cav3.2 Determines Low-Threshold Mechanoreceptor Function.
GINIP, a Gαi-Interacting Protein, Functions as a Key Modulator of Peripheral GABAB Receptor-Mediated Analgesia.
Acute heat-evoked temperature sensation is impaired but not abolished in mice lacking TRPV1 and TRPV3 channels.
Uncoupling of Molecular Maturation from Peripheral Target Innervation in Nociceptors Expressing a Chimeric TrkA/TrkC Receptor.
Peripheral pain-sensing neurons: from molecular diversity to functional specialization.
TAFA4, a Chemokine-like Protein, Modulates Injury-Induced Mechanical and Chemical Pain Hypersensitivity in Mice
Heterogeneity in primary nociceptive neurons: from molecules to pathology.
stac1 and stac2 genes define discrete and distinct subsets of dorsal root ganglia neurons.
Hepatocyte growth factor-Met signaling is required for Runx1 extinction and peptidergic differentiation in primary nociceptive neurons.
TRPV3 in keratinocytes transmits temperature information to sensory neurons via ATP.
Impaired thermosensation in mice lacking TRPV3, a heat and camphor sensor in the skin.
Expressing TrkC from the TrkA locus causes a subset of DRG neurons to switch fate.
Actualités
Découvrez comment les membres de notre institut impactent le grand public grâce à des initiatives de vulgarisation et des projets créatifs.
Plusieurs projets portés par nos équipes ont été sélectionnés pour un financement par l’ANR et la FRM, mettant en lumière leur travail et leur recherche innovante.
La dysbiose du microbiote intestinal favorise la douleur somatique chronique chez les souris mâles déficientes en Myo1a.
La spin-off de l’IBDM récompensée pour son innovation dans un médicament non opioïde pour le soulagement de la douleur.
Nous avons montré qu’après SPNS, des neurones inhibiteurs de la lamina II interne (LIIi) et des neurones excitateurs de la lamina II externe (LIIo) présentent des altérations d’un courant K+ transitoire (IA) qui augmente dans des neurones inhibiteurs de la LIIi et diminue dans des neurones excitateurs de la LIIo.
Ardem Patapoutian, shares the honours of his Nobel Prize with his former post-docs and students
Ardem Patapoutian shares the honours of his Nobel Prize with his former post-docs and students including Aziz Moqrich, Chronic pain : Molecular and cellular mechanisms
Tafalgie Therapeutics, une nouvelle start-up issue des travaux de l’équipe d’Aziz Moqrich
Issue des travaux de l’équipe d’Aziz Moqrich « douleur chronique : mécanismes cellulaires et moléculaires », Tafalgie Therapeutics est une nouvelle start-up créée en novembre 2020.
Loss of bhlha9 impairs thermotaxis and formalin-evoked pain in a sexually dimorphic manner
Dans une étude publiée dans Cell Reports, Bohic et al. confirment le rôle des C-LTMR dans la modulation de la douleur inflammatoire en inactivant le facteur de transcription bhlha9.
Conditions requises : Maîtrise en physique, biophysique, acoustique, biologie moléculaire ou cellulaire, neurosciences ou dans une discipline connexe.